Содержание
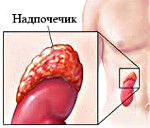
Адреногенитальный синдром (АГС) — симптомокомплекс, развивающийся в результате дисфункции коры надпочечников. Для этой формы патологии используют также другой термин — врожденная дисфункция коры надпочечников (ВДКН).
Адреногенитальный синдром относится к нейроэндокринным син-дромам условно, т. к. эта патология является следствием хромосомной мутации, что приводит к дефициту ферментных систем, участвующих в синтезе стероидных гормонов надпочечников. При этой патологии нарушается синтез кортизола, по принципу обратной связи возрастает образование АКТГ в гипофизе и усиливает синтез предшественников кортизола, из которых, вследствие дефицита фермента, образуется не кортизол, а андрогены. Избыток андрогенов определяет развитие характерных для заболевания проявлений.
Различают следующие формы АГС:
Врожденная форма адреногенитального синдрома.
Гиперпродукция андрогенов начинается внутриутробно с началом гормональной функции надпочечников (9–10 неделя внутриутробной жизни). В этот период жизни внутренние половые органы уже имеют четкую половую принадлежность, а наружные половые органы находятся на стадии формирования. Под влиянием избытка тестостерона происходит вирилизация наружных половых органов: половой бугорок увеличивается, превращаясь в пенисообразный клитор, сливаются лабиосакральные складки, приобретая вид мошонки, урогенитальный синус не разделяется на уретру и влагалище, а персистирует и открывается под пенисообразным клитором. Поскольку гонады имеют женское строение, а наружные — мужское, эта патология класси-фицируется как ложный женский гермафродитизм. Такая вирилизация приводит к неправильному определению пола при рождении ребенка.
В зависимости от клинического течения врожденную форму АГС разделяют на:
Чаще встречается вирильная форма. При рождении ребенка нередко ошибаются в определении пола — девочку с врожденным АГС принимают за мальчика. Отличительная особенность: хромосомный набор всегда 46ХХ, матка и яичники развиты правильно.
В первом десятилетии жизни у девочек с врожденной формой АГС развивается картина преждевременного полового созревания по гетеросексуальному типу. Гиперандрогения благодаря анаболическому действию андрогенов стимулирует развитие мышечной и костной ткани. Благодаря хорошему развитию мышечной ткани дети с врожденным АГС выглядят как «маленькие Геркулесы».
При сольтеряющей форме АГС у новорожденных также выражены симптомы гиперандрогенизации, однако они менее выражены, чем при вирильной форме. У пациенток с данной формой АГС нарушен синтез не только глюкокортикоидов, но и минералокортикоидов, поэтому на первый план в клинической картине выступают проявления нарушений обмена электролитов.
Гипертоническая форма АГС редко встречается и диагностируется поздно. Степень гипертонии зависит от выраженности дефекта синтеза гормонов надпочечников.
Диагностика. Повышенное содержание ДЭА в крови, нормализующееся после проведения пробы с глюкокортикоидными препаратами.
Лечение. Дети с врожденной формой АГС являются пациентами эндокринологов, тактика их лечения разработана, что позволяет вовремя произвести коррекцию и направить дальнейшее развитие по женскому типу. С целью коррекции гормональной функции надпочечников используются глюкокортикоидные препараты, терапию проводят длительно, так как дефицит ферментной системы имеет врожденный характер. При грубой вирилизации наружных половых органов производится пластическая операция.
Пубертатная форма адреногенитального синдрома.
Быстрый рост. При этой форме АГС избыточное образование андрогенов начинается с наступления полового созревания, что совпадет с периодом физиологической активации надпочечников, в т. н. период адренархе, по времени на 2–3 года опережающий менархе — наступление менструаций. Физиологическое увеличение секреции андрогенов в этом возрасте обеспечивает так называемый «скачок роста» и появление полового оволосения. Для девочек с данной патологией характерны:
— телосложение спортивного типа: широкие плечи, узкий таз;
— гипертрихоз: как правило, единичные стержневые волосы над верхней губой, на щеках, бедрах;
— менархе у большинства — с 14–16 лет, менструации носят нерегулярный характер, при этом характер менструального цикла и гипертрихоз четко коррелируют с гиперандрогенией: чем выше уровень андрогенов, тем реже менструации;
— молочные железы гипопластичны.
Дата добавления: 2018-11-24 ; просмотров: 142 ; ЗАКАЗАТЬ РАБОТУ
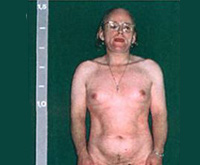
Адреногенитальный синдром — наследственное заболевание надпочечников, при котором вследствие функциональной несостоятельности ферментов нарушается стероидогенез. Проявляется вирилизацией гениталий, маскулиноподобным телосложением, недоразвитием груди, гирсутизмом, акне, аменореей или олигоменореей, бесплодием. В ходе диагностики определяют уровни 17-гидроксипрогестерона, 17-кетостероидов, андростендиона, АКТГ, проводят УЗИ яичников. Пациенткам назначают заместительную гормонотерапию глюкокортикоидами и минералокортикоидами, эстрогены в комбинации с андрогенами или прогестинами нового поколения. При необходимости выполняют пластику половых органов.
МКБ-10
Общие сведения
Адреногенитальный синдром, или врожденная дисфункция (гиперплазия) коры надпочечников, — наиболее частое из наследуемых заболеваний. Распространенность патологии отличается у представителей разных национальностей. Классические варианты АГС у лиц европеоидной расы встречаются с частотой 1:14 000 младенцев, в то время как у эскимосов Аляски этот показатель составляет 1:282. Существенно выше заболеваемость у евреев. Так, неклассическую форму адреногенитального расстройства выявляют у 19% лиц еврейской национальности группы ашкенази. Патология передается по аутосомно-рецессивному типу. Вероятность рождения ребенка с таким синдромом при носительстве патологического гена у обоих родителей достигает 25%, в браке носителя и больного — 75%. Если один из родителей имеет полноценные ДНК, клинические проявления синдрома у детей не развиваются. При наличии АДС у отца и матери ребенок также будет болен.

Причины адреногенитального синдрома
У больных с наследуемой гиперплазией надпочечников генетический дефект проявляется несостоятельностью ферментных систем, участвующих в секреции стероидных гормонов. В 90-95% случаев патология возникает при повреждении гена, который отвечает за синтез 21-гидроксилазы — фермента, влияющего на образование кортизола. В остальных клинических случаях вследствие дефекта ДНК нарушается производство других ферментов, обеспечивающих стероидогенез, — StAR/20,22-десмолазы, 3-β-гидрокси-стероиддегидрогеназы, 17-α-гидроксилазы/17,20-лиазы, 11-β-гидроксилазы, P450-оксидоредуктазы и синтетазы альдостерона.
У пациентов с признаками вирилизирующего синдрома вместо активного гена CYP21-B в коротком плече 6-й аутосомы расположен функционально несостоятельный псевдоген CYP21-A. Структура этих участков ДНК-цепи во многом гомологична, что повышает вероятность конверсии генов в мейозе с перемещением участка нормального гена на псевдоген или делецию CYP21-B. По-видимому, именно этими механизмами объясняется существование скрытых форм болезни, дебютирующих в пубертате или постпубертатном периоде. В таких случаях клинические признаки патологии становятся заметными после нагрузок, истощающих кору надпочечников: тяжелых болезней, травм, отравлений, радиационных воздействий, длительного периода интенсивной работы, психологически напряженных ситуаций и т. д.
Патогенез ВДКН
В основе механизма развития наиболее распространенного варианта адреногенитального синдрома с дефектом CYP21-B-гена лежит принцип обратной связи. Ее начальным звеном становится дефицит стероидов — кортизола и альдостерона. Несостоятельность процессов гидроксилирования сопровождается неполным переходом 17-гидроксипрогестерона и прогестерона в 11-дезоксикортизол и дезоксикортикостерон. В результате снижается секреция кортизола, а для компенсации этого процесса в гипофизе усиливается синтез АКТГ — гормона, вызывающего компенсаторную гиперплазию коры надпочечников для стимуляции выработки кортикостероидов.
Параллельно возрастает синтез андрогенов и появляются видимые признаки их влияния на чувствительные ткани и органы. При умеренном снижении активности фермента минералокортикоидная недостаточность не развивается, поскольку потребность организма в альдостероне почти в 200 раз ниже по сравнению с кортизолом. Только глубокий дефект гена вызывает тяжелую клиническую симптоматику, которая проявляется с раннего возраста. Патогенез развития заболевания при нарушении структуры других участков ДНК аналогичен, однако пусковым моментом являются нарушения в других звеньях стероидогенеза.
Классификация
Систематизация различных форм вирилизирующей гиперплазии надпочечников основана на особенностях клинической картины заболевания, выраженности генетического дефекта и времени проявления первых патологических признаков. Тяжесть расстройства напрямую связана со степенью повреждения ДНК. Специалисты в сфере эндокринологии различают следующие виды адреногенитального синдрома:
- Сольтеряющий. Самый тяжелый вариант патологии, проявляющийся в первый год жизни ребенка грубыми нарушениями строения наружных половых органов у девочек и их увеличением у мальчиков. Активность 21-гидроксилазы составляет не более 1%. Значительное нарушение стероидогенеза приводит к выраженным соматическим нарушениям — рвоте, поносу, судорогам, чрезмерной пигментации кожи. Без лечения такие дети умирают в раннем возрасте.
- Простой вирильный. Течение заболевания менее тяжелое, чем при сольтеряющем варианте. Преобладают проявления неправильного развития гениталий у младенцев женского пола, увеличение их размеров у мальчиков. Признаки надпочечниковой недостаточности отсутствуют. Уровень активности 21-гидроксилазы снижен до 1-5%. С возрастом у пациентов нарастают признаки вирилизации вследствие стимулирующего действия андрогенов.
- Неклассический (постпубертатный). Наиболее благоприятная форма АГС, явные признаки которой возникают в период полового созревания и в репродуктивном возрасте. Наружные половые органы имеют нормальное строение, может быть увеличен клитор у женщин и половой член у мужчин. Функциональность 21-гидроксилазы снижена до 20-30%. Заболевание выявляется случайно при обследовании в связи с бесплодием или нарушениями менструальной функции.
Сольтеряющий и простой вирильный виды адреногенитальных расстройств относят к категории антенатальной патологии, формирующейся внутриутробно и проявляющейся с момента рождения. При дефекте строения других генов наблюдаются более редкие варианты заболевания: гипертензивные — классический (врожденный) и неклассический (поздний), гипертермический, липидный, с ведущими проявлениями гирсутизма.
Симптомы адреногенитального синдрома
При антенатальных формах заболевания (простой вирильной и сольтеряющей) основным клиническим симптомом является видимая вирилизация гениталий. У новорожденных девочек обнаруживаются признаки женского псевдогермафродитизма. Клитор большой по размерам или имеет пенисообразную форму, преддверие влагалища углублено, сформирован урогенитальный синус, большие и малые половые губы увеличены, промежность высокая. Внутренние половые органы развиты нормально. У младенцев-мальчиков увеличен половой член и гиперпигментирована мошонка. Кроме того, при сольтеряющем адреногенитальном расстройстве выражена симптоматика надпочечниковой недостаточности с тяжелыми, зачастую несовместимыми с жизнью соматическими нарушениями (понос, рвота, судороги, обезвоживание и др.), которые проявляются с 2-3-недельного возраста.
У девочек с простым вирильным АГС по мере взросления признаки вирилизации усиливаются, формируется диспластическое телосложение. Из-за ускорения процессов окостенения пациентки отличаются невысоким ростом, широкими плечами, узким тазом, короткими конечностями. Трубчатые кости массивные. Половое созревание начинается рано (до 7 лет) и протекает с развитием вторичных мужских половых признаков. Отмечается увеличение клитора, снижение тембра голоса, нарастание мышечной силы, формирование типичной для мужчин формы перстневидного хряща щитовидной железы. Грудь не растет, менархе отсутствует.
Менее специфичны клинические симптомы при неклассических формах вирилизирующего синдрома, возникшие в пубертате и после стрессовых нагрузок (выкидыша на ранних сроках беременности, медицинского аборта, операции и др.). Обычно пациентки вспоминают, что у них еще в младшем школьном возрасте появилось небольшое оволосение в подмышечных впадинах и на лобке. В последующем развились признаки гирсутизма с ростом стержневых волос над верхней губой, по белой линии живота, в области грудины, в сосково-ареолярной зоне. Женщины с АГС предъявляют жалобы на стойкую угревую сыпь, пористость и повышенную жирность кожи.
Менархе наступает поздно — к 15-16 годам. Менструальный цикл неустойчив, интервалы между менструациями достигают 35-45 дней и более. Кровянистые выделения во время месячных скудные. Молочные железы небольшие. Клитор несколько увеличен. Такие девушки и женщины могут иметь высокий рост, узкий таз, широкие плечи. По наблюдениям специалистов в сфере акушерства и гинекологии, чем позже развиваются адреногенитальные расстройства, тем менее заметны внешние признаки, характерные для мужчин, и тем чаще ведущим симптомом становится нарушение месячного цикла. При более редких генетических дефектах пациентки могут жаловаться на повышение артериального давления или, наоборот, гипотонию с низкой работоспособностью и частыми головными болями, гиперпигментацию кожи с минимальными симптомами вирилизации.
Осложнения
Основным осложнением адреногенитального синдрома, по поводу которого пациентки обращаются к акушерам-гинекологам, является стойкое бесплодие. Чем раньше проявилось заболевание, тем меньше вероятность забеременеть. При значительной ферментной недостаточности и клинических проявлениях простого вирилизирующего синдрома беременность вообще не наступает. У забеременевших пациенток с пубертатными и постпубертатными формами заболевания возникают самопроизвольные выкидыши на раннем сроке. В родах возможна функциональная истмико-цервикальная недостаточность. Такие женщины более склонны к возникновению психоэмоциональных расстройств — склонности к депрессии, суицидальному поведению, проявлениям агрессии.
Диагностика
Постановка диагноза при антенатальных типах АГС с характерными изменениями половых органов не представляет сложности и проводится сразу после родов. В сомнительных случаях применяют кариотипирование для подтверждения женского кариотипа (46ХХ). Большее значение диагностический поиск приобретает при позднем клиническом дебюте или скрытом течении с минимальными внешними проявлениями вирилизации. В подобных ситуациях для выявления адреногенитального синдрома используют следующие лабораторные и инструментальные методы:
- Уровень 17-ОН-прогестерона. Высокая концентрация 17-гидроксипрогестерона, который является предшественником кортизола — ключевой признак недостаточности 21-гидроксилазы. Его содержание увеличено в 3-9 раз (от 15 нмоль/л и выше).
- Стероидный профиль (17-КС). Повышение уровня 17-кетостероидов в моче у женщин в 6-8 раз свидетельствует о высоком содержании андрогенов, производимых корой надпочечников. При выполнении преднизолоновой пробы концентрация 17-КС уменьшается на 50-75%.
- Содержание андростендиона в сыворотке крови. Повышенные показатели этого высокоспецифичного метода лабораторной диагностики подтверждают усиленную секрецию предшественников мужских половых гормонов.
- Уровень АКТГ в крови. Для классических форм заболевания характерна компенсаторная гиперсекреция адренокортикотропного гормона передней долей гипофиза. Поэтому при синдроме вирилизирующей дисфункции показатель повышен.
- УЗИ яичников. В корковом веществе определяются фолликулы на разных стадиях созревания, не достигающие преовуляторных размеров. Яичники могут быть несколько увеличены, однако разрастания стромы не наблюдается.
- Измерение базальной температуры. Температурная кривая типична для ановуляторного цикла: первая фаза растянута, вторая укорочена, что обусловлено недостаточностью желтого тела, которое не образуется из-за отсутствия овуляции.
Для сольтеряющего варианта АГС также характерна повышенная концентрация ренина в плазме крови. Дифференциальная диагностика адреногенитальных расстройств, возникших в пубертатном и детородном возрасте, проводится с синдромом поликистозных яичников, овариальными андробластомами, андростеромами надпочечников, вирильным синдромом гипоталамического происхождения и конституциональным гирсутизмом. В сложных случаях к диагностике привлекают эндокринологов, урологов, врачей-генетиков.
Лечение адреногенитального синдрома
Основным способом коррекции вирильной дисфункции надпочечников является заместительная гормональная терапия, восполняющая дефицит глюкокортикоидов. Если у женщины со скрытым АГС нет репродуктивных планов, кожные проявления гиперандрогении незначительны и месячные ритмичны, гормоны не применяют. В остальных случаях выбор схемы лечения зависит от формы эндокринной патологии, ведущей симптоматики и степени ее выраженности. Зачастую назначение глюкокортикоидных препаратов дополняют другими медикаментозными и хирургическими методами, подобранными в соответствии с конкретной терапевтической целью:
- Лечение бесплодия. При наличии планов по деторождению женщина под контролем андрогенов крови принимает глюкокортикоиды до полного восстановления овуляторного месячного цикла и наступления беременности. В резистентных случаях дополнительно назначают стимуляторы овуляции. Во избежание выкидыша гормонотерапию продолжают до 13-й недели гестационного срока. В I триместре также рекомендованы эстрогены, во II-III — аналоги прогестерона, не обладающие андрогенным эффектом.
- Коррекция нерегулярных месячных и вирилизации. Если пациентка не планирует беременность, но жалуется на расстройство менструального цикла, гирсутизм, угри, предпочтительны средства с эстрогенным и антиандрогенным эффектом, оральные контрацептивы, содержащие гестагены последнего поколения. Терапевтический эффект достигается за 3-6 месяцев, однако по окончании лечения при отсутствии заместительной гормонотерапии признаки гиперандрогении восстанавливаются.
- Лечение врожденных форм АГС. Девочкам с признаками ложного гермафродитизма проводят адекватную гормонотерапию и выполняют хирургическую коррекцию формы половых органов — клитеротомию, интроитопластику (вскрытие урогенитального синуса). При сольтеряющих адреногенитальных расстройствах кроме глюкокортикоидов под контролем рениновой активности назначают минералокортикоиды с увеличением терапевтических доз при возникновении интеркуррентных заболеваний.
Определенные сложности в ведении пациентки возникают в тех случаях, когда заболевание не диагностировано в акушерском стационаре, и девочка с выраженной вирилизацией гениталий регистрируется и воспитывается как мальчик. При решении о восстановлении женской половой идентичности хирургическую пластику и гормонотерапию дополняют психотерапевтической поддержкой. Решение о сохранении гражданского мужского пола и удалении матки с придатками принимается в исключительных случаях по настоянию больных, однако такой подход считается ошибочным.
Прогноз и профилактика
Прогноз при своевременном обнаружении адреногенитального синдрома и адекватно подобранной терапии благоприятный. Даже у пациенток со значительной вирилизацией гениталий после пластической операции возможна нормальная половая жизнь и естественные роды. Заместительная гормонотерапия при любой форме АГС способствует быстрой феминизации — развитию грудных желез, появлению месячных, нормализации овариального цикла, восстановлению генеративной функции. Профилактика заболевания осуществляется на этапе планирования беременности.
Если в роду наблюдались случаи подобной патологии, показана консультация генетика. Проведение пробы с АКТГ обоим супругам позволяет диагностировать гетерозиготное носительство или скрытые формы адреногенитального расстройства. При беременности синдром может быть обнаружен по результатам генетического анализа клеток хорионических ворсин или содержимого околоплодных вод, полученных методом амниоцентеза. Неонатальный скрининг, проводимый на 5-е сутки после родов, направлен на выявление повышенной концентрации 17-гидропрогестерона для быстрого выбора терапевтической тактики.
Адреногенитальный синдром (АГС, врожденная дисфункция коры надпочечников) – заболевание, вызываемое наследственно обусловленным дефицитом ферментов, регулирующих образование гормонов надпочечников, чаще 21-гидроксилазы, приводящее к нарушению синтеза кортизола (простая форма) или кортизола и альдостерона (сольтеряющая форма), проявляющееся нарушениями соматического развития и минерального обмена.
Этиология: наследственное заболевание по аутосомно-рецессивному типу.
А) простая форма – нарушен синтез только ГКС
Б) сольтеряющая форма – нарушен синтез ГКС и минералкортикоидов.
Патогенез простой формы АГС:
Патогенез развития сольтеряющей формы АГС отличается более выраженным дефицитом 21-гидроксилазы, приводящим к нарушению синтеза не только кортизола, но и альдостерона,
А) простой формы – симптомы зависят от пола, у мальчиков при рождении практически отсутствуют, в дальнейшем характерно ускорение роста и созревания скелета, раннее завершение процесса роста, преждевременное половое созревание по мужскому типу; у девочек при рождении происходит вирилизация половых органов (гипертрофия клитора и больших половых губ), в дальнейшем ускорение роста и созревание скелета, раннее половое созревание по мужскому типу (маскулинизация тела, отсутствие молочных желез, гирсутизм).
Б) сольтеряющей формы – в первые дни жизни проявляется аналогична простой, после второй недели жизни состояние ребенка прогрессивно ухудшается, наблюдается рвота, отказ от еды, потеря массы тела, сонливость, адинамия, тахикардия (обусловлены потерей хлористого натрия и развитием сольдефицитного эксикоза), без лечения развивается кома и больной погибает.
Диагностика АГС: данные семейного анамнеза (нарушение полового развития у родственников, сочетание низкорослости с бесплодием, рано умершие новорожденные с неправильным строением гениталий), клиники, повышение экскреции 17-КС с мочой, повышенние уровня 17-гидроксипрогестерона и АКТГ в крови; при сольтеряющей форме также выявляют признаки эксикоза, гипохлоремию и гиперкалиемию
При простой форме – заместительная терапия ГКС в течение всей жизни больного (преднизолон 4-10 мг/м2 тела/сут в 3-4 приема), у девочек в 3-4-летнем возрасте выполняют хирургическую пластику наружных гениталий.
В остром периоде сольтеряющей формы заболевания показаны солезамещающие растворы (изотонический раствор хлористого натрия, раствор Рингера и пр.) и 5-10% раствор глюкозы в соотношении 1:1 в/в капельно до 150-170 мл/кг массы тела/сут, гормональная терапия гидрокортизоном гемисукцинатом / солукортеф 10-15 мг/кг/сут, разделенной на 4-6 в/в или в/м введений. В случаях возникновения стрессовых ситуаций (интеркурентное заболевание, травма, операция и т. п.) доза ГКС повышается в 1,5-2 раза во избежание развития острой надпочечниковой недостаточности (гипоадреналового криза). Если терапию проводят преднизолоном, то одновременно в/м вводят дезоксикортикостерона ацетат (ДОКСА) по 10-15 мг/сут, в дальнейшем дозу ДОКСА снижают, вводят через день или два.

При рано начатом и регулярно проводимом лечении дети развиваются нормально, при сольтеряющей форме АГС прогноз хуже, дети нередко погибают на 1-м году жизни.