Содержание
- 1 Виды терапии
- 2 Процедура проведения
- 3 Плюсы терапии
- 4 Возможные осложнения
- 5 Вывод
- 6 Как избежать осложнений после брахитерапии рака предстательной железы?
- 7 Что нельзя делать после возникновения осложнений брахитерапии рака предстательной железы?
- 8 Какие лечебные мероприятия могут помочь при возникновении побочных эффектов брахитерапии?
- 9 Выбор тактики лечения
- 10 Изменения тканей простаты при облучении
- 11 Диагностика и проведение контактной терапии
- 12 Особенности проведения процедуры
- 13 Показания и противопоказания
- 14 Что делать после брахитерапии

Одним из видов радиотерапии, применяемым для максимально точного введения излучения в поражённую зону органа, является брахитерапия. Брахитерапия при раке простаты используется на начальных этапах заболевания и основывается на индивидуальном подходе к отдельному случаю.
Доброго вам здоровья, уважаемые читатели. Это Александр Бурусов, и в этой статье вы познакомитесь с таким методом терапии при раке простаты как брахитерапия, так же вы узнаете, какие осложнения она может вызывать.
Сразу отмечу, что при назначении этого метода лечения специалисты обращают внимание на возраст пациента, степень заболевания, а также возможность осложнений после лучевой терапии (классификация по степени риска). Важно, что такое лечение переносится гораздо легче, чем операции или дистанционные облучения.
Виды терапии
Брахитерапия при лечении рака предстательной железы (РПЖ) относится к радикальным методам лечения, но даже консервативно настроенные специалисты видят в нём эффективность и безопасность. Ведь главное преимущество заключается в том, что большая доза лучей направлена непосредственно на опухоль, а нежелательное воздействие на не поражённые органы и ткани сведено к минимуму.
Обязательное условие: объём простаты не должен превышать стандартных размеров, иначе вводимая игла не достигнет цели, а риск осложнений может повыситься. Уменьшить объём простаты возможно с помощью гормональной терапии, которая проводится в среднем в течение 5 месяцев. Только после уменьшения объёма железы возможно проведение брахитерапии.
Эффективность лечения рака предстательной железы зависит от своевременного выявления заболевания, поэтому необходимо регулярно проходит медицинские осмотры.
Процедура проведения
Первый этап брахитерапии заключается в планировании. Врач должен на основе показаний УЗИ, МРТ или КТ установить наиболее оптимальные параметры терапии. Сюда входят: дозировка облучения, количество вводимых в простату так называемых «зёрен» с радиоактивным йодом, а также точное место их введения.
После этого устанавливается метод лечения, их всего 2:
- низкодозная брахитерапия;
- высокодозная брахитерапия.
В первом случае лечение проводится с помощью введения в простату капсул. Длится такая терапия около 2 часов. Заранее очищается кишечник, а во время проведения пациент находится либо под полным наркозом, либо под неполным, который подразумевает обезболивание только нижней части тела.
Пациент располагается на спине в фиксированной позе с  согнутыми коленями, а в это время в полость раковой опухоли вводится ультразвуковой прибор для контроля изображения на мониторе.
согнутыми коленями, а в это время в полость раковой опухоли вводится ультразвуковой прибор для контроля изображения на мониторе.
После этого в простату вводятся «зёрна» через специальные иглы, которые затем вынимаются. Введённые капсулы при использовании постоянной брахитерапии остаются в организме на всю жизнь.
Затем начинается период облучения раковых клеток (в течение 2 месяцев), когда опухоль уменьшается в размерах, а затем совсем исчезает. В этот период не нужно постоянное наблюдение врача, а пациент может быть выписан из больницы в тот же день, как была проведена брахитерапия.
Во втором случае принцип действия тот же, но капсулы находятся в простате в течение 15 минут, а затем удаляются. Концентрация радиоактивности «зёрен» выше, чем при низкодозной брахитерапии, а значит оставлять капсулы на долгое время в организме пациента нельзя во избежание осложнений. Такая лучевая терапия проводится исходя из отмеченных специалистом индивидуальных особенностей случая заболевания.
Плюсы терапии
- малая продолжительность процедуры и восстановительного периода. Если терапия проведена без последующих осложнений, то пациент может заниматься привычной деятельностью уже в последующую неделю после проведения процедуры;
- высокая степень сохранения потенции;
- сведение травматичности к минимуму. После имплантации не наблюдается осложнений ректального характера, а также проблем с мочеиспусканием;
- хорошая переносимость пациентами. Брахитерапия отлично переносится людьми в возрасте, а также теми, кто параллельно болен другими заболеваниями;
- результативность. После применения данного вида лечения сохраняется оптимальное качество жизни пациента.
Возможные осложнения
После процедуры брахитерапии пациент может чувствовать необоснованную утомляемость, аллергические реакции на коже (зуд, покраснение), отмечается воспаление мочевого пузыря (цистит), кровь в моче, а также воспаление пищевого тракта. Возможна диарея, нарушение мочеиспускания, понижение эрекции.
Не исключено сужение мочевого канала, вероятны отёки ног, незначительное выпадение волос в паху. Эти последствия брахитерапии рака простаты могут проявлять себя по отдельности и в разное время, почти никогда в совокупности и одновременно.
Непосредственно после проведения операции в течение нескольких дней ранки от вводимых игл могут кровоточить, а в моче наблюдаться наличие кровяных сгустков. Такая реакция организма приемлема и не стоит бить тревогу.
Нужно употреблять больше жидкости, что бы произошло  самоочищение организма, а кровь вышла естественным путём. Ранки же можно обрабатывать антиаллергенными мазями с заживляющим эффектом, но они не приносят особого беспокойства и быстро проходят сами собой.
самоочищение организма, а кровь вышла естественным путём. Ранки же можно обрабатывать антиаллергенными мазями с заживляющим эффектом, но они не приносят особого беспокойства и быстро проходят сами собой.
Проблемы с мочеиспусканием, в частности недержание мочи, встречается крайне редко. Зато проблемы с эрекцией наблюдаются почти у 35% мужчин, что впоследствии может привести к полной импотенции. Не исключены трудности с опорожнением кишечника, может наблюдаться появление слизи в фекалиях.
Такие трудности с испражнениями обычно проходят через несколько недель без вмешательства специалистов или медикаментозного лечения. Не стоит бояться радиоактивности капсул, так как она имеет малый радиус действия на организм человека.
Не исключено, что после методов радикального лечения болезнь может вернуться, что является довольно частым явлением. По статистике биохимический рецидив рака простаты выявляется у одной трети больных РПЖ. Это зависит от этапа и расположения раковой опухоли, а также от показателя уровня простатического специфического антигена (ПСА), который не должен превышать 0,2 нг/мл.
Также в расчёт берётся история изменений и совокупность метастазов в лимфоузлах. Рецидивирование может образоваться как в самой простате, так и в прилегающих к ней тканях. Не исключено и поражение других органов, в первую очередь в группе риска находятся лёгкие и кости.
Вывод
Лечить рецидив нужно в соответствии с проводимой ранее терапией. Цель лечения заключается в устранении новообразования с последующим улучшением состояния пациента, избавлением от симптомов, нежелательных эффектов и избеганием летального исхода. В случае если пациент проходил лучевое лечение, повторное облучение поражённой опухолью зоны не рекомендуется.
Также развитие рецидивирующего рака может быть остановлено на несколько лет с помощью гормональной терапии. Главный минус такого лечения в том, что со временем раковая опухоль начинает расти, что говорит о гормонально-резистивной опухоли. Такая стадия рецидива неизлечима, а пациенты с наблюдаемыми осложнениями живут около года.
Возможно проведение химиотерапии, которая уменьшает интенсивность проявления симптомов, облегчая самочувствие пациента. На протяжении трёх лет отмечается стабилизация и улучшение общего состояния больного. Современными методами терапии рецидива являются криохирургическая и радиочастотная аблация, а также усовершенствованная система применения ультразвука.
Брахитерапия относится к наиболее востребованным методам лечения рака предстательной железы. В первую очередь интерес к этому методу продиктован небольшим количеством возможных осложнений, возможностью сохранения потенции, низким риском недержания мочи, которая отмечается у каждого пятого больного, прошедшего хирургическое лечение.
Тем не менее, и брахитерапия, в некоторых случаях, может привести к развитию побочных эффектов:
- Затруднение мочеиспускания.
Самым частым осложнением после брахитерапии рака предстательной железы является затруднение мочеиспускания, которое отмечается у 1%-5% больных . Как правило, задержка мочеиспускания (обструктивные нарушения) после брахитерапии возникает у больных с аденомой предстательной железы, которая вызывает заметные нарушения мочеиспускания еще до начала лучевого лечения. Поэтому, все больные раком предстательной железы пред проведением брахитерапии проходят тщательное обследование (урофлоуметрия, определение объема остаточной мочи, заполнение специальных опросников).Это позволяет выделить ту группу больных, которым проведение лучевого лечения рака предстательной железы не желательно из-за повышенного риска осложнений. Остальным пациентам лечение может быть выполнено без значительного риска возникновения побочных эффектов. - Нарушения со стороны прямой кишки.
Вторым, наиболее частым осложнением после брахитерапии рака предстательной железы являются нарушения со стороны прямой кишки, которые проявляются в виде болевых ощущений, явлений постлучевого воспаления, кровянистых выделений из прямой кишки. Наиболее часто эти побочные эффекты наблюдаются после проведения дистанционной лучевой терапии (по данным некоторых авторов, их частота достигает 10%-15% ). Несколько реже, подобные осложнения возникают после, так называемой, низкодозной (классической) брахитерапии
Как избежать осложнений после брахитерапии рака предстательной железы?
Наиболее эффективно указанные задачи помогает решать самый современный вариант брахитерапии – высокодозная брахитерапия. За счет точного подведения запланированной дозы на предстательную железу и небольшой лучевой нагрузки на окружающие нормальные ткани высокодозная брахитерапия позволяет снизить риск осложнений со стороны прямой кишки до минимума ( 0%-2% ).
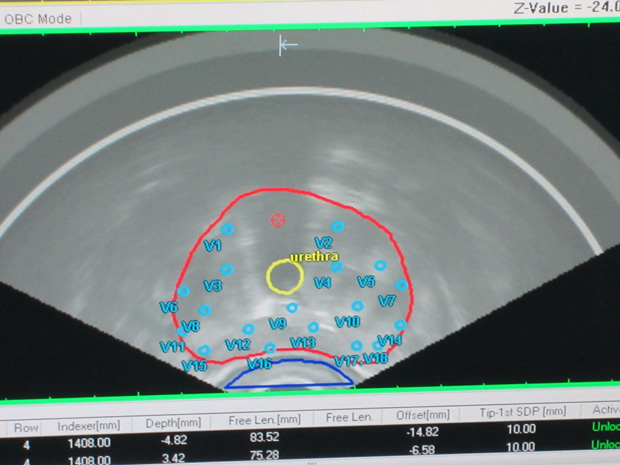
Кроме того, при таком лечении обеспечиваются наиболее благоприятные условия для сохранения у пациентов потенции и снижается риск возникновения недержания мочи с 15%-20% (хирургическое лечение) до 0%-1% . Эти особенности высокодозной брахитерапии позволяют достигать выздоровления больных раком предстательной железы при сохранении нормальной жизненной активности и минимальном риске возникновения тяжелых побочных эффектов лечения.
Например, по данным специалистов НИИ онкологии им. Н.Н. Петрова, которые провели более 500 сеансов высокодозной брахитерапии, риск возникновения серьезных нарушений мочеиспускания составил 1.1% (в основном, эти осложнения отмечались у больных, прошедших трансуретральную резекцию аденомы предстательной железы), осложнений со стороны прямой кишки — менее 1%, случаев недержания мочи зарегистрировано не было.
Что нельзя делать после возникновения осложнений брахитерапии рака предстательной железы?
Нередко, пациенты, прошедшие лучевое лечение рака предстательной железы, в том числе, брахитерапию, при возникновении осложнений попадают на лечение в поликлинику или стационары общей лечебной сети. В этом случае, больным нередко предлагают хирургические методы лечения:
- трансуретральную резекцию при нарушениях мочеиспускания,
- биопсию стенки прямой кишки — при осложнениях со стороны прямой кишки.
Следует помнить, что любые инвазивные (хирургические) манипуляции на уретре, мочевом пузыре, прямой кишке после проведения брахитерапии крайне нежелательны. Они могут выполняться только после предварительной консультации с Вашим лечащим врачом-радиотерапевтом.
Какие лечебные мероприятия могут помочь при возникновении побочных эффектов брахитерапии?
В большинстве случаев осложнения брахитерапии имеют временный преходящий характер. Они возникают в течение первых нескольких недель и стихают в течение последующих нескольких месяцев. При длительном сохранении нежелательных последствий, как правило, используются лекарственные методы лечения. Например, при затруднении мочеиспускания назначаются препараты из группы альфа-блокаторов, при наличии болей в области прямой кишки — активно используются противовоспалительные препараты, свечи, мази и т.д.

Авторская публикация:
НОВИКОВ СЕРГЕЙ НИКОЛАЕВИЧ
радиолог, онколог, радиотерапевт
ведущий научный сотрудник, заведующий отделением
НИИ онкологии им Н.Н. Петрова
Особенностью терапии является то, что в рамках лечения ткани не страдают, то есть метод брахитерапии является малоинвазивным и высокоточным.

В урологии брахитерапия все чаще применяется для лечения онкологии простаты и показывает в этом хорошую эффективность. В зависимости от общего состояния тканей больного, контактная терапия может быть самостоятельной или комбинированной.
Действие осуществляется при помощи узконаправленного облучения, то есть терапия поражает исключительно раковые клетки, не оказывая пагубного влияния на окружающие ткани.
Но минусом метода является то, что оборудование и специалисты для брахитерапии есть далеко не в каждом медицинском учреждении.
Выбор тактики лечения
Перед тем, как начать лечение рака любого типа, врач направляет пациента на обследование и онкоконсилиум, в рамках которого специалисты принимают решение о выборе тактики лечения и дальнейших мерах.
Медики учитывают такие факторы, как количество баллов по Глисону (должно быть не больше 7) и стадия ракового процесса (Т1 и Т2).
Согласно проводимым научным исследованиям, узконаправленное облучение тканей дает лучшие результаты, чем традиционное хирургическое вмешательство.
Брахитерапия не оказывает столь травмирующего влияния на организм, как операция и иссечение тканей. Брахитерапия при раке простаты условно разделяется на два вида – высокодозную и низкодозную.

Высокодозная брахитерапия
Для лечения по методу HDR применяются иридиум-192 или цезиум-137. Высокодозная терапии длится на протяжении небольшого количества времени.
Это стало возможным за счет интенсивного облучения повышенной мощности. Во время терапии изотопы вводятся в пораженные ткани в четко определенной локации, затем они извлекаются.
HDR назначается в различных целях:
- перед плановой операцией с целью снижения размеров опухоли до приемлемого уровня;
- при агрессивной форме онкологии.
Высокодозное облучение дает возможность уменьшить размеры локализации болезни, снизить количество рецидивов. При этом лечение менее вредно для мужского здоровья, чем стандартная лучевая терапия дистанционного типа.
Изотопы в ткани предстательной железы вводятся при помощи специальной иглы, длительность высокодозного облучения составляет примерно 10 минут. При введении соблюдается определенный интервал между изотопами: обычно это 3 мм.
При необходимости сеанс повторяется второй и даже третий раз, если врач считает это необходимым.

Низкодозная брахитерапия
Для проведения такого типа контактного лечения используются йод-125 и палладиум-103. Процесс лечения предполагает имплантирование зерен изотопов в пораженные ткани на длительный период.
Обычно время лечения составляет 6 месяцев, после чего радиоактивные зерна нейтрализуются, то есть они перестают быть источниками постоянного низкодозного облучения.
Введение изотопов осуществляется при помощи специальных роботизированных инструментов с максимальной точностью. Для введения применяется контроль МРТ, общее количество которых разно 50 микрокапсулам, что является достаточным для эффективного лечения.
Перед тем, как начать терапию, врач оценивает объем и состояние простаты, определяет точную локализацию пораженной области. Доза необходимого изучения рассчитывается автоматически при помощи программных методов, что обеспечивает точность облучения.
При введении микрокапсул используется обезболивание, поэтому пациент не испытывает сильного дискомфорта. Длительность процедуры – примерно 50-60 минут, лучевая нагрузка — 120 Грей.
Низкодозная терапия обладает многими преимуществами, например, именно такой метод позволяет мужчине сохранить эректильную функцию примерно в 85% случаев.
Но это справедливо только тогда, когда ранее никаких проблем с потенцией не было. Кроме того, после облучения не нарушается мочеиспускание, что связано с особенностями терапии.

В отличие от обычной лучевой терапии негативное влияние облучения на организм сводится к минимуму, катетеризация мочевого пузыря не требуется. Но эффект от проводимой терапии наступает не сразу, а спустя определенное время.
Изменения тканей простаты при облучении
Проводимая брахитерапия предстательной железы дает первые заметные результаты уже через пару месяцев после начала терапии.
Опухолевое образование вместе с простатой значительно уменьшается в объеме, но ПСА (простатический специфический антиген) в этот период может немного увеличиться. Это нормальная ситуация, спровоцированная воспалительными процессами при проведении лучевой терапии.
Анализы крови на ПСА следует повторно сделать через 3 месяца после окончания сеансов облучения. Ультразвуковое обследование также назначают только через 2-3 месяца, чтобы не спровоцировать увеличение простаты.
Сами результаты облучения через пару месяцев свидетельствуют об улучшении состояния здоровья, уменьшении объема пораженных тканей.
Показатели уровня простат-специфического антигена также снижаются, но больному все равно требуется регулярный контроль динамики ПСА.
Анализы крови должны прийти к уровню, соответствующему периоду до начала лечения. В противном случае можно говорить о прогрессировании опухолевого процесса. В этом случае специалист назначает дополнительное обследование и выбирает дополнительные методы лечения.

Диагностика и проведение контактной терапии
Перед началом процедуры необходимо провести диагностику, сделать расчет разовой, суммарной дозы воздействия на организм. Врач при проведении подобного исследования обращает внимание на такие факторы:
- общая масса тела больного;
- общем железы (до 50 куб. м);
- локализация опухолевой ткани, объем пораженных тканей;
- показания анализа ПСА;
- трансуретральная резекция в анамнезе (ТУР);
- наличие дизурических расстройств;
- наличие сопутствующих патологий;
- проводимая ранее терапия, включая лучевую.
Брахитерапия простаты может проводиться только после утверждения ее целесообразности. Поле этого специалист назначает обследование, определяет метод контактного облучения и дозировку.
Комплекс исследований направлен на подтверждение диагноза, оценки распространения опухоли, вероятность исключения появления метастаз в будущем.

Пациенту назначаются следующие виды обследований;
- общие анализы мочи, крови;
- анализ на биохимию крови;
- ультразвуковое обследование почек, мочевого пузыря, брюшной полости, мошонки;
- сцинтиграфия (проводится для костей скелета);
- рентгенография легких (необходим снимок в двух проекциях);
- МРТ органов малого таза;
- результаты проводимой трансректальной биопсии, которые подтверждают диагноз, дают представление о злокачественности опухоли.

Особенности проведения процедуры
Поле получения снимков в формате 3D врач имеет возможность распланировать процедуру, определить требуемый вид терапии, дозу облучения, количество радиоактивных зерен для введения в ткани. Пациент во время процедуры должен лежать на кушетке на спине, ноги следует развести в сторону.
Для контроля выполняемых манипуляций используется ультразвуковой аппарат, что позволяет максимально точно ввести изотопы.
- При низкодозном лечении изотопы вводятся специальными высокоточными иглами-проводниками. Область введения находится между предстательной железой и мошонкой. После окончания манипуляции иглы удаляются.
- При высокодозной терапии применяется другое оборудование, во время манипуляции необходима установка радиоизотопных катетеров, через которые изотопы доставляются в пораженную локацию. После окончания сеанса катетеры удаляются вместе с радиоактивными микрокапсулами.
Показания и противопоказания
Контактное облучение относится к узконаправленным воздействиям, снижающим риск негативного влияния на организм. Но это не означает, что окружающие ткани не затрагиваются вообще.
По этой причине терапия проводится только при соблюдении следующих условий:
- новообразование имеет индекс до 8 (при комбинированном лечении);
- значение по шкале Глисона не должно превышать 7;
- радиус проникновения равен 1,5-2 мм, т.е. при запущенной форме заболевания процедура может быть неэффективна;
- при уровне ПСА от 15-20, выраженных обструктивных расстройствах мочеиспускания, вовлечении в процесс семенных пузырьков и проводимой ранее ТУР резекции брахитерапия не проводится.

Процедура может вызвать у пациента такие негативные последствия, как слабость, общая интоксикация, головная боль.
Но все эти симптомы быстро проходят после окончания терапии и не несут вред для организма. Исключения включают в себя дизурические и эректильные расстройства, фиброз простаты, лучевой проктит.
К положительным аспектам лечения относятся:
- снижение риска рецидива;
- отсутствие необходимости в госпитализации;
- в 96% случаев отмечается выздоровление (при 1, 2 стадиях рака);
- повторное лечение не назначается;
- реабилитация занимает минимум времени;
- риск осложнений и негативных последствий минимальный;
- процесс лечения не влияет на потенцию (если с этим не было проблем ранее);
- выживаемость пациентов в течение 10 лет после окончания терапии составляет 86%.
Что делать после брахитерапии
Пациент после проводимого лечения должен придерживаться следующих правил:
- нельзя поднимать тяжести более 5 кг;
- нельзя загорать и долго находиться на солнце;
- физиотерапевтические процедуры проводить нельзя;
- необходима строгая диета с исключением спиртного, соленого, кислого, острого;
- с собой требуется всегда носить справку о проводимом лечении, чтобы исключить проблемы при прохождении металлоискателя;
- необходим регулярный контроль ПСА (каждые три месяца);
- сауну и баню посещать нельзя;
- требуется контроль мочеиспускания, стула;
- первое время рекомендуется мочиться в емкость, так как имплантат может выйти сам.
Брахитерапия является одним из наиболее эффективных и безопасных методов лечения рака. В большинстве случаев нет никаких осложнений. Также пациент может заниматься сексом, потому что негативного влияния на потенцию нет.
© 2018 — 2019, Еганов Еган Павлович. Все права защищены.